La química Casi Todo
lunes, 17 de agosto de 2015
Tipos de Reacciones Quimicas
1- Reacciones de Síntesis o Adición
Las reacciones de síntesis o adición son aquellas donde las substancias se juntan formando una única sustancia. Representando genéricamente los reactivos como A y B, una reacción de síntesis puede ser escrita como:
A + B —– > AB
2- Reacciones de Análisis o Descomposición
Las reacciones de análisis o descomposición son lo opuesto de las reacciones de síntesis, o sea, un reactivo da origen a productos más simples que el. Escribiendo la reacción genérica nos resulta fácil entender lo que sucede:
AB —– > A + B
3- Reacciones de Desplazamiento
Las reacciones de desplazamiento o de sustitución simple merecen un poco más de atención que las anteriores. No que sean complejas, pues no lo son, pero tienen algunos pequeños detalles. En su forma genérica la reacción puede ser escrita como:
AB + C —– > A + CB
4- Reacciones de Doble Sustitución
Son también muy simples, pero debemos quedar atentos a los detalles. El mecanismo es fácil:
AB + CD —– > AD + CB
Clasificacion De Enlaces Covalente
a) enlace covalente simple: Cada átomo aporta un electrón al enlace, es decir, se comparte un par de electrones entre dos átomos. Un ejemplo es la molécula de Hidrógeno (H2):
b) enlace covalente doble: Cada átomo aporta dos electrones al enlace, es decir, se comparten dos pares de electrones entre dos átomos. Un ejemplo es la molécula de Oxígeno (O2):
c) enlace covalente triple: Cada átomo aporta tres electrones al enlace, es decir, se comparten tres pares de electrones entre dos átomos, por ejemplo, la molécula de Nitrógeno (N2).
ii) atendiendo a cómo están compartidos los electrones:
Enlace covalente apolar a) enlace covalente puro o apolar: Los dos átomos que comparten electrones son del mismo elemento o bien de elementos de la misma electronegatividad para que los electrones enlazantes se compartan por igual. Todos los ejemplos vistos hasta ahora son de este tipo.
b) enlace covalente polar: En un enlace covalente entre dos átomos iguales, los electrones del enlace se hallan igualmente compartidos, y el caso del enlace iónico constituye el otro extremo en el que los e‑ se transfieren totalmente.
c) enlace covalente coordinado o dativo: Es un enlace covalente en el que el par de e‑ que se comparte es aportado por un solo átomo. A los compuestos con este tipo de enlace se llaman complejos

b) enlace covalente doble: Cada átomo aporta dos electrones al enlace, es decir, se comparten dos pares de electrones entre dos átomos. Un ejemplo es la molécula de Oxígeno (O2):
c) enlace covalente triple: Cada átomo aporta tres electrones al enlace, es decir, se comparten tres pares de electrones entre dos átomos, por ejemplo, la molécula de Nitrógeno (N2).
ii) atendiendo a cómo están compartidos los electrones:
Enlace covalente apolar a) enlace covalente puro o apolar: Los dos átomos que comparten electrones son del mismo elemento o bien de elementos de la misma electronegatividad para que los electrones enlazantes se compartan por igual. Todos los ejemplos vistos hasta ahora son de este tipo.
b) enlace covalente polar: En un enlace covalente entre dos átomos iguales, los electrones del enlace se hallan igualmente compartidos, y el caso del enlace iónico constituye el otro extremo en el que los e‑ se transfieren totalmente.
c) enlace covalente coordinado o dativo: Es un enlace covalente en el que el par de e‑ que se comparte es aportado por un solo átomo. A los compuestos con este tipo de enlace se llaman complejos
El nuemero de Avogadro
En química y en física, la constante de Avogadro (símbolos: L, NA) es el número departículas elementales (usualmente átomos o moléculas) en un mol de una sustancia cualquiera, donde el mol es una de las siete unidades básicas del Sistema Internacional de Unidades (SI). Su dimensión es el recíproco del mol y su valor es igual a 6,022 140857(74)×1023 mol−1


Geometría Molecular
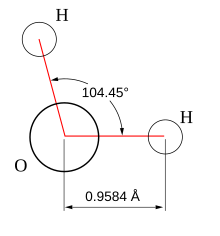
La geometría molecular o estructura molecular se refiere a la disposición tridimensional de los átomos que constituyen una molécula. Determina muchas de las propiedades de las moléculas, como son la reactividad, polaridad, fase, color,magnetismo, actividad biológica, etc. Actualmente, el principal modelo de geometría molecular es la Teoría de Repulsión de Pares de Electrones de Valencia (TRPEV), empleada internacionalmente por su gran predictibilidad.

Suscribirse a:
Entradas (Atom)